抗癌新药拉罗替尼为什么这样牛?
文章来源:向日葵儿童 作者:向日葵前沿小组 责任编辑:admin 时间:2018-12-21
作者 | 周叶斌,AbbVie 研发人员;
Ethan,马什菲尔德诊所儿科住院医师;
霍子荷,瑞士巴塞尔儿童医院肿瘤病理博士在读
要说最近最火、风头最盛的抗癌药,一定是拉罗替尼(Larotrectinib)莫属了,但是它到底有什么特殊的地方吸引了这么多目光呢?
1、新药开发过程与众不同:这是第一个研发和临床实验完全只基于一个分子特征来完成的抗癌药。
2、批准上市过程弯道超车:因为针对的靶点相对小众,所以这个药物不仅通过FDA“快速审批通道”上市,还被认定为“孤儿药”,这在抗癌药里是很罕见的。
3、药物未来走向依旧未知:这个药物目前披露出来的临床数据量很小但是效果很好,大家也都很关注其后续发展。
4、药物上市影响十分深远:拉罗替尼上市这件事情本身又一次向大众推广了“靶向药物”“精准医疗”这两个概念,为以后新的抗癌药研发提供了不同的思路和范例。
现在我们就从这几个点来详细为大家介绍拉罗替尼到底有啥不一样!
这次药物开发的特别之处是什么?
拉罗替尼与其他传统肿瘤药物研发最大的区别是,这个药整个的研发和临床试验都是基于一个分子——NTRK融合基因来进行的,并没有具体限制在某种肿瘤中。
这样的研发方式在历史上是第一次。
其实,癌症中的分子标记早已用在了抗癌药的研发上。比如大名鼎鼎的乳腺癌药赫赛汀就是基于有些乳腺癌表达的Her2蛋白。
但不同的是,以前抗癌药的研发虽然也基于某个分子标记,但还是限制在某些肿瘤里,比如赫赛汀就只针对乳腺癌。
而这次的拉罗替尼只对NTRK融合基因有要求,没有限定具体是什么癌,所以获批的适用人群里也只对分子标记有要求。

这次药物的批准上市过程有何不同?
拉罗替尼被FDA指定为“突破性治疗”后走了快速审批通道。像最近很火的PD-1/PD-L1单抗也都走过这个“快车道”。
这个“快车道”其实就是FDA把有些还在临床试验中的新药指定为“突破性治疗”,一般是指对于目标人群目前没有更好的治疗方法,并且对治疗改善可能有巨大作用的潜在新药,得到这样指定的新药在审批时速度会更快。
另外,走这个通道还有一个很大的优势是,审批时可以只有临床试验中总体缓解率(ORR)或者无进展生存期(PFS)数据,不需要最后总体生存期(OS)的数据。
【总体缓解率(ORR)是治疗后有缓解的患者比例,无进展生存期(PFS)就是癌症患者的病情没有恶化的时间,总体生存期(OS)是指患者在使用某个药物后的存活时间。】
不难看出,在一个临床试验里,总体缓解率数据(ORR)最容易获得,无进展生存期数据(PFS)的取得也要比总体存活率早得多。
但如果从药物的实际效果考虑,总体生存期(OS)更重要。因此,即便通过“快车道”审批上市,FDA也会要求药企继续进行临床试验,补充总体生存期(OS)的数据,证明药物确实能够延长患者生命。
同时,由于拉罗替尼针对的NTRK基因融合的患者人群很小,因此,还被FDA同时认定为“孤儿药”,这在抗癌药的批准上市中也是很罕见的。
【作者有话说:在总体生存期(OS)这个问题上,最近获批的一些新药也给FDA带来了一定挑战。有些抗癌药在通过“快车道”获批后,最后总体生存期(OS)并没有提高,FDA目前也还没有把这些药撤回来,确实有点尴尬。】
03
作为FDA认定的“突破性治疗”,拉罗替尼目前的临床数据只做到了总体缓解率(ORR)。在报批时,Loxo与拜耳把所有拉罗替尼的小规模临床试验数据整合在一起,用这个结果拿到了上市许可。
这个数据量有多小呢?三个临床试验加在一起总共只有176个患者(都有NTRK基因融合,包括44个儿童),并且所有的数据都用在证明拉罗替尼的安全性了。
药物有效性的结果是从最早进入试验的55个患者里得出的(后面患者的治疗效果数据还没出来)。这55个患者得出的是总体缓解率是75%,其中,22%是完全缓解。缓解持续时间的数据还没完全出来,超过6个月的是73%,其中有39%的患者缓解时间超过一年。
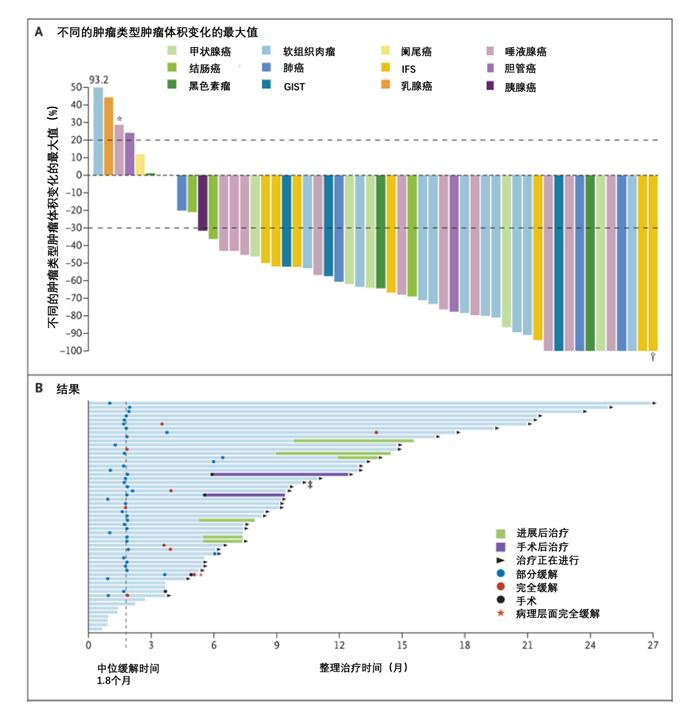
怎么评价这些数据呢?
首先,这些数据确实有让人眼前一亮的地方。毕竟总体缓解率达到75%是很高的,证明拉罗替尼对有NTRK基因融合的患者确实有效,特别是这些患者很多本身是没有其他治疗方式可选的。
但另一方面,这个数据量确实很小。我们还不知道最终患者缓解的时间会有多长,多久会出现耐药性,能否真正延长患者生命,缺少的这些数据恰恰是我们整体判断一个抗癌药的重要指标。
因此,我们也不要急着为拉罗替尼“封神”,最后的结果还需要更多的临床数据以及时间的检验。
未来是否会有更多类似的广谱抗癌药出现?
会。首先是拉罗替尼这种只看分子标记,不管肿瘤发生位置的研发模式会有人继续尝试。
Loxo本身就在继续这样的研发道路,他们还有针对RET基因融合的产品正在进行临床试验,患者的录入标准就是有RET基因融合的实体瘤患者,并没有限定具体肿瘤类型。
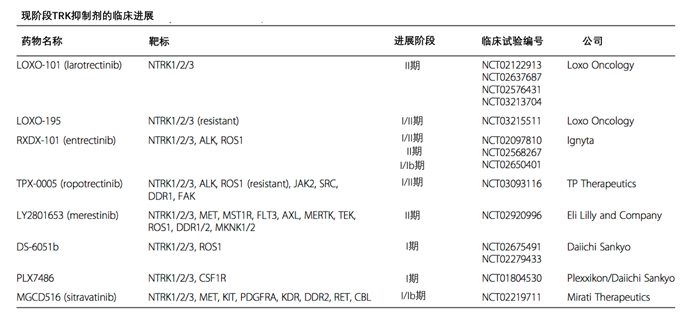
此外,关于拉罗替尼的耐药性研究也已提上日程,Loxo另一个产品就是肿瘤出现对拉罗替尼耐药后的下一代NTRK抑制剂。关于NTRK,制药巨头罗氏也有一个类似拉罗替尼的药在临床试验中,目前得到的数据与拉罗替尼非常接近,预计离上市也不远。
比如默克的PD-1单抗Keytruda连续在皮肤癌、肺癌等癌症的治疗中取得成功后,著名肿瘤学家Vogelstein猜测这类药物可能对于基因突变多的癌症效果特别好。
默克根据这个假说,做了针对具有微卫星不稳定的遗传标记的癌症患者的临床试验,结果发现只要带有这种分子标记,不论肿瘤来源,Keytruda的治疗效果都很好。
Keytruda也凭这个试验结果成功获得了治疗带有微卫星不稳定的癌症的审批,成了第一个“广谱抗癌药”。
此外,关于大家都很关心的儿童实体瘤,也有一些着重关注的靶点,以后可能就会针对这些靶点进行新药开发。
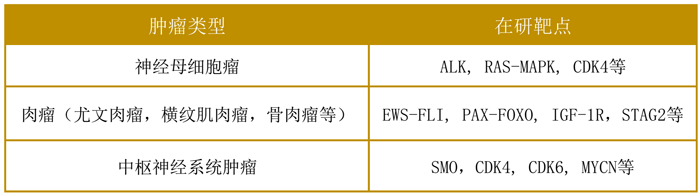
类似拉罗替尼的广谱抗癌药是否会成为主流?
有可能,但有难度。
这个困难存在于两个层面,一个是找到在一种肿瘤中的发挥作用的关键分子尚且不易,更别说是找到一个在多种肿瘤中都很关键的分子,并且还要研发出针对这个分子的特异性药物,这个难度是非常大的。
另一方面,只基于某个分子不考虑肿瘤发生组织的治疗方案未必可靠。美国国立卫生研究院(NIH)下属的癌症研究所开展了根据癌症患者的分子特征分类,而不是基于组织分类用药的试验,但之前公布的结果并不理想。
但无论如何,拉罗替尼这样的创新性抗癌药的上市依然有着重大意义,至少它给很多患者带来了希望。
参考文献
Chen Y, and Chi P. Basket trial of TRK inhibitors demonstrates efficacy in TRK fusion-positive cancers. J Hematol Oncol. 2018;11(1):78.
2. Drilon A, Laetsch TW, Kummar S, DuBois SG, Lassen UN, Demetri GD, et al. Efficacy of Larotrectinib in TRK Fusion-Positive Cancers in Adults and Children. N Engl J Med. 2018;378(8):731-9.
3. Tran TH, Shah AT, and Loh ML. Precision Medicine in Pediatric Oncology: Translating Genomic Discoveries into Optimized Therapies. Clin Cancer Res. 2017;23(18):5329-38.
4. 4. https://www.clinicaloncology.com/FDA-Watch/Article/11-18/FDA-Approves-Vitrakvi-for-Solid-Tumors-With-NTRK-Gene-Fusions/53466
往期推荐:
保健品与药同服,有时反而有害
“抗癌新药”法舒克终于在国内上市!
新靶点可有效抑制神母肿瘤生长
儿童肿瘤很可怕?有些却能自愈!
为什么中国儿童无药可吃
相关文章
“抗艾滋婴儿”并不能抵抗艾滋
“抗艾滋婴儿”预防艾滋师出无名,所谓的“技术制高点”也并没有任何突破。
肿瘤患儿疫情期间就诊需注意什么?
在这个特殊的时期,孩子的就诊和复查需要注意些什么呢?我们整理了北上广深医院公告。
孙凌霞营养师:癌症患儿营养的三个关键期怎么破?
孙凌霞老师在“国际儿童癌病日”科普论坛分享癌症患儿的营养护理。
2月15日国际儿童癌病日科普巡讲即将开启
每年的2月15日,世界各地都会为国际儿童癌症日(ICCD)进行宣传活动。
哪些措施可以预防蒽环类药物的心脏毒性?
这一期,我们将着重介绍儿科常用广谱化疗药——蒽环类药物的药物基因组学研究。








