骨肉瘤
文章来源:向日葵儿童网站 作者:不明 责任编辑:admin 时间:2018-10-31
基本信息
骨肉瘤是最常见的骨原发恶性肿瘤类型,约占儿童肿瘤的5%。骨肉瘤主要发生于青少年 。常发生于骨骼快速生长的部位,如长骨的干骺端(干骺端是骨干和骨骺的交界处),以膝关节上下,即股骨远端和胫骨近端常见,其次为肱骨近端。但事实上骨肉瘤能在任意骨骼中发生,包括骨盆(髋)、肩部和下颌。
目前骨肉瘤的主要治疗手段为手术结合化疗为主的综合治疗。骨肉瘤恶性程度较高,常发生转移,其中以肺转移为主。15岁以下患者的5年生存率约76%,15-19岁患者的5年生存率约为66%。
病因及风险因素
1. 病因
对大多数的骨肉瘤病例来说,其确切病因尚不知晓。一些基因的突变被认为和发病的风险有关。
2. 风险因素
任何增加患病风险的因素都被称为风险因素。有风险因素并不意味着一定会得肿瘤;没有风险因素并不意味着一定不会得肿瘤。
骨肉瘤的风险因素包括:
(1)年龄:
10-30岁之间的年龄群体发生骨肉瘤的风险最高,特别是青少年的发育爆发期,这提示了快速骨骼生长与肿瘤发生风险之间有一定的联系。
(2) 身高:
患有骨肉瘤的儿童比同龄人身材偏高,同样提示骨肉瘤可能与快速骨骼生长相关。
(3) 性别:
骨肉瘤多见于男性。如女性发病,多倾向于在更早年龄阶段发生,可能是因为她们的身高突增期更早。
(4)过去曾用放射疗法治疗:
接受过治疗其他肿瘤的放疗的患者会有更高的风险在放疗区域附近发展出骨肉瘤。在年幼时接受高剂量的辐射会增加骨肉瘤发生的风险。
(5)过去曾用蒽环类或烷基化剂的化疗药物治疗。
(6)RB1基因有特定的变化。
(7)具有以下遗传性综合征的患者:
- Bloom症(布卢姆综合征):罕见的单基因常染色体隐性遗传病,由BLM基因突变引起,症状为身材矮小,易患肿瘤。
- Diamond-Blackfan贫血(先天性纯红细胞再生障碍性贫血):以贫血为主要表现,并累及多系统组织的遗传病。
- Li-Fraumeni综合征(李-法美尼综合征):多数由遗传的抑癌P53突变引起,患者容易发展数类肿瘤,包括乳腺癌、脑部恶性肿瘤、骨肉瘤以及其他类型肉瘤。
- Paget病(佩吉特病):一种起源于皮内或皮下腺体的罕见皮肤癌,多表现为类似于皮炎的皮肤潮红、渗出、结痂。
- 遗传性视网膜母细胞瘤:起源于视网膜(眼球壁的感光层)的一种眼部恶性肿瘤,可发生于单眼或双眼。
- Rothmund-Thomson综合征(先天性血管萎缩皮肤异色病):由REPL4基因突变引起,是一种累及多系统的遗传病,出生后3-6个月即发病,典型起始症状为面颊处出现红色水肿型斑片,并可发展至其他部位,患者头发、眉毛、睫毛稀少。
- Werner综合征(白内障-硬皮病-早老综合征):是一种罕见遗传病,又名早老矮小病、成人早老综合征、成人早衰症等,典型症状为皮肤呈老年貌,毛发灰白及脱落,眼部发生白内障,身材矮小,发育停顿。
可以看出,绝大多数已知的危险因素都是先天的,包括年龄、身高、种族、性别、特定骨骼疾病和遗传性综合征等。这些因素都无法被改变。除了放疗以外,并不清楚有哪些生活习惯或环境因素会导致骨肉瘤发生,所以目前尚无方法有效避免骨肉瘤的发生。
分类
不同骨肉瘤亚型可以通过X光成像和病理检查结果来鉴别。其中一部分亚型相较其他有更好的预后。根据其病理结果,骨肉瘤可被分为:高级别、中级别或低级别。肿瘤分级提示肿瘤细胞生长和扩散的能力。
1. 高级别骨肉瘤
属于骨肉瘤中快速生长的种类。在显微镜下,它们与正常骨骼有差异,并且有许多正处于分裂期的细胞。大多数发生于儿童和青少年的骨肉瘤为高级别。
高级别骨肉瘤有很多类型(前三类最常见):
- 成骨细胞型
- 成软骨细胞型
- 成纤维细胞型
- 混合型
- 小细胞型
- 毛细血管扩张型
- 高级别表面型或高级别皮质旁型
其他高级别骨肉瘤包括:
- 佩吉特病样型:发生于佩吉特病患者骨骼中的肿瘤
- 骨外型:非骨骼处(而是在身体其他部位)发生的肿瘤
- 放射后型:发生于曾接受过放疗的骨骼的肿瘤
2. 中级别骨肉瘤
这部分不常见的肿瘤类型被划分在高级别和低级别之间(常被当作低级别骨肉瘤来治疗):
- 骨膜型或中级别皮质旁型
3. 低级别骨肉瘤
生长最慢的骨肉瘤类型。在显微镜下肿瘤与正常骨骼相似度较高,且含有更少处于分裂期的细胞。
- 骨膜外型或低级别皮质旁型
- 髓腔内或骨内高分化型或低级别中央型
临床表现
1. 骨或关节部位疼痛
肿瘤所累及的骨骼处(通常在膝盖或是上臂周围)有疼痛感是骨肉瘤最常见的症状。在最初,疼痛可能并不是持续的,只在晚上变得严重(称夜间痛)。在运动时这种疼痛常常会加重。
2. 局部肿块及或软组织肿胀
患处附近变得肿胀是骨肉瘤的另一个常见的现象,肿胀往往是在骨痛开始后的几周才会发生。根据肿瘤产生的位置不同,可能会摸到肿块或局部的隆起。
3. 不明原因的骨折(病理性骨折)
虽然骨肉瘤会使所累及的骨骼变得脆弱,但是这部分骨骼一般不会断裂。而毛细血管扩张性骨肉瘤虽然极少发生,但是这种骨肉瘤却比其他骨肉瘤对骨骼的影响更大,使肿瘤累及的骨骼变得更加脆弱,从而更有可能发生骨折或者骨断裂。
检查及诊断
1. 诊断策略
骨肉瘤的诊断遵循临床、影像、病理三结合。多数病例建议行MDT(多学科联合会诊),进行诊断并治疗。
2. 常见检查
- 身体检查和询问病史:检查身体的一般情况,检查疾病的体征,包括肿块或者其他异常。病史询问包括过去患过的疾病、治疗情况以及家族病史。
- 全血细胞计数(CBC):部分患者可出现贫血等表现。需要抽血检查红细胞、白细胞和血小板的数量;红细胞中血红蛋白的量(血红蛋白是携带氧气的蛋白质)、红细胞在血样中所占的比例等。
- 血液生化:生化检查中碱性磷酸酶在骨肉瘤患者中常出现升高。 需要抽血检测身体器官和组织释放到血液中的某些物质的量。某种物质含量异常(高于或低于正常水平)可能是疾病的征兆。这项测试是为了检查肝脏和肾脏的功能是否正常。
- X射线:可观察肿瘤生长的部位、大小等,肿瘤处在片子上显得凹凸不平而不是实心状,也可能呈现为骨内空洞。有时候医生能够观察到骨内缺损附近的肿瘤向周边组织(如肌肉或脂肪组织)延伸。通过X射线可见典型的骨膜反应,包括Codman三角及日光散射样骨膜反应。胸部X射线可用于判断骨肉瘤是否已经扩散至肺部。
- CT扫描:从各个断层对肿瘤进行检查,并可行三维成像及增强扫描观察肿瘤血液循环情况及肿瘤与血管关系。
- MRI:磁共振对于肿瘤界限及水肿带的显示具有优势。
- PET-CT扫描或骨扫描:有助于在全身范围内寻找肿瘤。该技术结合正电子发射断层扫描(PET)和计算机断层扫描(CT),两者同时在同一台机器上进行,将两种图像组合在一起,产生比两个测试本身更详细的图像。检查中将少量放射性葡萄糖注入静脉,拍摄葡萄糖在体内的摄取情况。在图像中恶性肿瘤细胞相对于正常细胞表现得更亮,因为它们比正常细胞更活跃,吸收更多的葡萄糖。
- 放射性核素骨扫描:用于检查骨骼中是否有快速分裂的细胞,如肿瘤细胞。极少量的放射性物质被注射到静脉中并通过血液运输全身。放射性物质会聚集在有肿瘤细胞的骨骼中,显示为密集、灰色至黑色的区域,称为“热点”。它可帮助提示肿瘤对骨骼造成多少伤害及是否已经扩散到其他骨骼。
- 活检:活检分为穿刺活检及切开活检。穿刺活检的优点是创伤小,但所获得诊断组织较小,诊断难度较大。切开活检对优点在于可获得足够的组织进行诊断,但是创伤较大,存在肿瘤污染风险。无论哪种活检都应注意取材通路,根治性手术时应将肿瘤与病理活检区域整块切除。
分期
用于查明肿瘤是否已经扩散到身体其他部位的过程称为分期。分期还与原发部位有关。对于骨肉瘤,大多数患者分期依据是肿瘤是否在身体的一个部分(局部)或者已经扩散(转移)。
骨肉瘤有几种分期方法,包括简单分期、Enneking外科分期方法和AJCC的TNM分期。
分期通常需要进行如下检查:
- X射线
- CT扫描
- PET-CT扫描:对骨转移的检测比骨扫描更灵敏和准确
- MRI核磁共振成像
- 骨扫描
1. 简单分期
根据制定治疗方案的需要,骨肉瘤可简单分为局部性和转移性肿瘤。
1.1 局部性骨肉瘤
没有扩散出发生肿瘤的骨骼。骨骼中可能存在一个或多个可以在手术过程中被移除的肿瘤区域。大约一半的肿瘤发生在股骨中,其中80%位于股骨远端。其他主要部位按频率降序排列为胫骨近端、肱骨近端、骨盆、颌骨、腓骨和肋骨。
1.2 转移性骨肉瘤
肿瘤从疾病开始的骨骼扩散到身体的其他部位。骨肉瘤最常扩散到肺部,也可能传播到其他骨骼。肿瘤可能从它开始的地方扩散到身体的其他部位称为转移。肿瘤细胞离开它们开始的地方(原发肿瘤),通过淋巴系统或血液传播。转移性肿瘤是与原发肿瘤相同类型肿瘤。例如,如果骨肉瘤扩散到肺,肺中的肿瘤细胞实际上是骨肉瘤细胞。该疾病是转移性骨肉瘤,不是肺癌。
2. Enneking外科分期(MSTS分期)
Enneking分期由肌肉骨骼系统肿瘤协会(Musculoskeletal Tumor Society, MSTS)制定,由三种关键信息来判定:
(1) 肿瘤分级(Grade, G):肿瘤分级是根据显微镜下图像、描述肿瘤生长和扩散能力的评估手段。肿瘤划分为低级别(G1)和高级别(G2)。低级别肿瘤细胞外观与正常细胞更为相似,并且较不容易快速生长和扩散,高级别肿瘤细胞其异型性更加明显,生长迅速,容易出现扩散。
(2) 肿瘤局部侵袭程度(Tumor, T): T1即局限型,说明肿瘤基本上还存在于骨骼内部;T2即侵犯型,说明骨骼已经延伸至骨骼之外,进入其他邻近结构。
(3) 肿瘤是否转移至邻近淋巴结或其他器官(Metastasized, M):尚未扩散至淋巴结或其他器官的肿瘤为M0,而发生扩散的为M1。
综合这些因素,并用罗马数字I至III编号,可以确定综合分期。I、II期还进一步地划分为A(局限型肿瘤)、B(侵犯型肿瘤)两类。
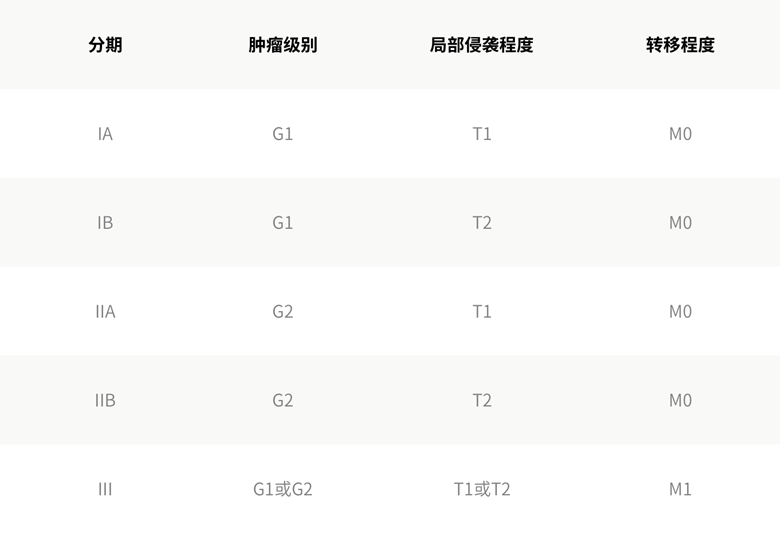
总的来说:
- 低级别、局部性肿瘤处于I期。
- 高级别、局部性肿瘤处于II期。
- 转移性肿瘤(不论哪种级别)处于III期。
3. TNM分期
美国肿瘤联合委员会(The American Joint Commission on Cancer,AJCC)系统给所有骨肉瘤进行了分期。其结合了4个因素用于分期,大写字母分别为:T、N、M和G。
- T代表肿瘤(Tumor)的特征(其尺寸以及是否在骨骼中不止一处存在);
- N代表向淋巴结(Lymph Node)侵袭;
- M代表向远端器官转移(Metastasis);
- G代表肿瘤分级(Grade)。
肿瘤分级基于镜检下细胞形态的异常程度,其级别越高,细胞形态越异常。高级别肿瘤相较于低级别肿瘤更倾向于快速地生长和转移。
将肿瘤特征、淋巴结侵袭、肿瘤转移和肿瘤分级的信息整合为一的过程就叫作分期分组。每一期可以进一步地被罗马数字划分为I至IV阶段。
3.1 骨肿瘤T分期
TX:原发肿瘤不能被测量出来
T0:无肿瘤存在迹象
T1:肿瘤不大于8厘米
T2:肿瘤大于8厘米
T3:在同一骨骼上肿瘤不止发生一次
3.2 骨肿瘤N分期
N0:肿瘤尚未转移至邻近淋巴结
N1:肿瘤已经转移至邻近淋巴结
3.3 骨肿瘤M分期
M0:肿瘤尚未转移至骨外或邻近淋巴结
M1:远端肿瘤转移(肿瘤已扩散)
M1a:肿瘤仅转移至肺部
M1b:肿瘤已经转移至其他部位(如脑、肝脏等)
3.4 骨肿瘤分级(G)
GX:无法归类
G1-G2:低级别
G3-G4:高级别
4. 复发
骨肉瘤最常在肺、骨或两者同时复发。骨肉瘤复发常发生在治疗完成后18个月内。
治疗
在过去的几十年里,骨肉瘤的治疗取得了长足的进步。在20世纪60年代,截肢是唯一的治疗方案,而且只有非常少数的患者确诊后能够存活两年以上。从那以后,医生们发现在手术之前和之后进行化疗能够治疗很多骨肉瘤患者,这也使得很多本需要截肢的患者得以进行保肢手术。
骨肉瘤的治疗包括标准治疗和临床试验。标准治疗指目前的常规疗法,大多数情况下,手术结合化疗为主要治疗方法。临床试验旨在改善目前的治疗或者获得关于新的治疗方法的信息。由于儿童恶性肿瘤罕见,如标准治疗方案效果不佳时,可以考虑参加临床试验。需注意,一些临床试验仅对未开始治疗的患者开放,因此需要及时与医生咨询和沟通。
1. 标准治疗方案
临床标准治疗以手术和化疗为主。
1.1 手术
手术的目的是在可能的情况下切除整个肿瘤。手术前可给予化疗使肿瘤缩小。因为若需要切除的骨组织减少,手术后的问题也相对减少。
手术类型包括:
1.1.1 广泛的局部切除
手术切除肿瘤和周围一些健康组织。
1.1.2 保肢手术
在不截肢的情况下切除患者肢体上(手臂或腿部)的肿瘤,因此保留了患者肢体的外观和功能。大多数四肢骨肉瘤患者可以用保肢手术治疗。同时也可以用患者自身身体的一部分组织和骨或人造骨,移植替换被移除的组织和骨。如果在诊断时、手术前或化疗期间出现骨折,在某些情况下仍然可能进行保肢手术。
1.1.3 截肢术
切除部分或全部手臂或腿部的手术。当患者肿瘤较大并侵及神经和(或)血管、不能在保肢手术中切除所有肿瘤时,可能会这样做。患者可在截肢后安装假肢。
1.1.4 旋转成形术
切除肿瘤和膝关节的手术。将保留的膝盖下方的腿代替移除的膝盖上方的腿的部分,然后脚朝后,踝关节起着膝盖的作用。之后再将假体附连到脚上(目前罕见)。
在手术移除可见的所有肿瘤后,患者可接受化疗以杀死可能残留在局部或扩散到身体其他部分的肿瘤细胞,以降低复发的风险,称为辅助治疗。
术后康复可能是所有治疗中不可或缺的一部分。患儿和他们的父母需要在术前和康复医师探讨治疗选择和术后需要进行的安排。如果是大腿截肢,患儿需要学习使用假肢生活。这对成长的儿童来说尤为困难,因为假肢需要时不时进行调整以跟上他们成长的步伐。在保肢手术后,有时面临的情况会更加复杂。成长期儿童可能需要更多后续手术更换内植物,以配合他们不断成长的体型。
1.2 化疗
化疗是一种常用的恶性肿瘤治疗方法,通过药物来杀死细胞或阻止细胞的繁殖,以此控制肿瘤细胞的生长。对大多数骨肉瘤患者,化疗是非常重要的治疗手段。
全身化疗是指药物通过口服或肌肉或静脉注射,药物进入血液并到达全身。局部化疗是指药物直接打入脑脊液\某个器官或者体腔(如腹腔),在局部发挥作用。
骨肉瘤患者多在切除原发肿瘤的手术前进行大约3个周期的化疗,称为新辅助化疗。手术后进行8个周期左右的化疗。
最常用的药物包括:甲氨蝶呤 (大剂量使用时同时采用亚叶酸来防止副作用)、阿霉素、顺铂或卡铂、表柔比星、异环磷酰胺、环磷酰胺、依托泊苷、吉西他滨或拓扑替康。
联合化疗是指同时使用一种以上的抗癌药物,常用的组合有:高剂量的甲氨蝶呤、阿霉素和顺铂 (有时是异环磷酰胺);阿霉素和顺铂;异环磷酰胺和依托泊苷;异环磷酰胺、顺铂 (或卡铂)和表柔比星。
2. 其他疗法
2.1 放射治疗
骨肉瘤患者可使用体外放射治疗,但由于该种肿瘤细胞不容易被放射治疗杀死,所以通常仅用于手术后杀死少量的遗留肿瘤,或和其他治疗合并使用。
一些新的放疗技术使得放疗的执行更为准确,包括三维适行放疗(three-dimensional conformal radiation therapy, 3D-CRT)、调强放疗(intensity modulated radiation therapy, IMRT)或质子适行放疗(conformal proton beam radiation therapy),这样的技术能够使得放疗医生更为确对准肿瘤进行照射,同时尽量减少肿瘤周围正常组织的受照剂量。因此,增加了治疗的成功率,同时减少了副作用。
钐是一种放射性元素,富集于骨细胞生长的区域。它有助于缓解由骨骼中的肿瘤引起的疼痛,并且杀死骨髓中的血细胞。它也用于治疗复发于其他骨上的骨肉瘤。用钐治疗后可能需要进行干细胞移植。在进行钐治疗之前,将健康的造血干细胞(未成熟血细胞)从患者的血液或骨髓中取出并冷冻保存。钐治疗完成后,将储存的干细胞解冻并输注回患者体内。这些重新注入的干细胞将恢复身体的造血功能。
2.2 靶向治疗
靶向治疗是利用药物或其他物质识别和攻击特定肿瘤细胞,且不伤害正常细胞的一种治疗方法。
有不同类型的靶向治疗用于治疗骨肉瘤或在临床试验中研究骨肉瘤的治疗:
2.2.1 激酶抑制剂:
2.2.2 mTOR抑制剂:
2.2.3 单克隆抗体:
抗体来自实验室制造出来的特定的免疫细胞。这些抗体可以识别肿瘤细胞上的物质,或者那些帮助肿瘤细胞生长的正常物质。抗体附着在目标物质上,杀死肿瘤细胞,阻止其生长或阻止其扩散。单克隆抗体通过输注给药。它们可以单独使用或携带其他药物、毒素或放射性物质到肿瘤细胞。Denosumab和Dinutuximab是正在研究的用于治疗复发性骨肉瘤的单克隆抗体。
2.3 临床试验
对于一些患儿来说,参加临床试验可能是最佳的治疗选择。临床试验是肿瘤研究过程的一部分,用以找出新的肿瘤治疗是否安全有效或优于标准治疗。当今许多肿瘤的标准治疗方法都是基于早期的临床试验。参加临床试验的患儿可以接受标准治疗,也可以直接接受新治疗。即使当临床试验没有带来有效的新治疗方法时,参与者也能够助推研究进程。患儿可以在治疗前、治疗中或治疗结束后进入临床试验。
需注意不同临床试验目的不同,针对的患者群体不同:一些试验只接受尚未进行任何治疗的患者;一些试验针对接受了标准治疗而未改善的患者;一些试验的目的是测试阻止复发或减少治疗的副作用。
参与临床试验可能需要进行多次测试,以观察治疗效果,用以决定是否继续、改变或停止治疗。后续测试检查发生在治疗结束后,主要观察患者的状态及肿瘤是否复发。
详情参阅网站 https://clinicaltrials.gov
3. 确定治疗方案
根据骨肉瘤的不同亚型选择对应的治疗方案,骨肉瘤的治疗方案取决于:
(1)肿瘤在体内的位置;
(2)肿瘤的大小;
(3)肿瘤的分期和分级;
(4)骨骼是否还在生长;
(5)患者的年龄和整体健康状况;
(6)患者和家属对患者是否能够参加诸如体育运动等活动的意愿,或对外观的要求;
(7)肿瘤是初次诊断的还是治疗后复发的。
3.1 局部骨肉瘤
治疗可包括以下内容:
- 手术切除原发肿瘤
- 化疗,可在切除原发肿瘤的手术前和(或)后进行
- 对那些不能进行手术或肿瘤没有被手术完全切除的患者可考虑给予放射治疗。
3.2 转移性骨肉瘤
骨肉瘤发生转移后,少数情况下可进行手术,如单发和极少数多发。在可手术的情况下,考虑以下方式:
3.2.1 肺转移
当骨肉瘤扩散时,它通常扩散到肺,治疗包括:
- 在原发肿瘤或者扩散到肺部的肿瘤细胞的切除手术后进行化疗。
3.2.2 骨转移或骨合并肺转移
骨肉瘤可扩散到远处骨和(或)肺,治疗可包括以下方案:
- 手术前进行化疗,然后手术切除原发肿瘤和已经扩散到身体其他部位的肿瘤,手术后给予更多化疗。
- 先手术切除原发肿瘤,随后进行化疗,并手术切除已经扩散到身体其他部位的肿瘤细胞。
3.3 复发性骨肉瘤
复发性骨肉瘤的治疗包括:
- 切除已经扩散到身体其他部位的肿瘤的手术
- 化疗
- 对于仅在骨中复发的肿瘤,单独使用钐,或联合患者自身的干细胞移植,以此缓解疼痛和改善生活质量
- 靶向治疗:尝试索拉非尼或依维莫司
- 一些新的临床试验:检查患者肿瘤样本是否有某些基因变化。可使用的靶向治疗的类型取决于基因改变的类型
- 针对不能通过手术切除肿瘤的患者的临床试验:包括靶向治疗如单克隆抗体治疗。
提示:
向日葵儿童提供的治疗相关信息仅供参考,不能替代医生和其他医务人员的建议,更不能取代医生的当面就诊。如果您有具体关于疾病,治疗方案,诊断或者临床症状的问题,请寻求专业医务人员帮助。
4. 治疗的副作用
4.1 骨肉瘤特定的可能副作用
- 骨骼肿胀,肿胀部分超过骨骼或身体的骨骼部分
- 骨骼或关节的疼痛
- 骨骼或关节发红或发热
- 关节僵硬或运动困难
- 身材矮小(比正常身高矮)
- 脊柱弯曲或脊柱后凸
- 骨质疏松(由于活动减少而导致的骨量丢失)
- 放射性骨坏死(尤其是髋关节或膝盖因血流不足坏死)
- 有日常生活活动方面的问题
- 不能像平常那样活跃
- 慢性疼痛或感染
- 假体安装或使用方面的问题
- 骨折
- 手术后骨骼可能无法痊愈
- 患肢比另一侧健肢短。
4.2 肿瘤治疗常见副作用
肿瘤治疗会引起副作用,因为杀灭肿瘤细胞的同时也会影响健康组织或器官,开始治疗后身体可能会有如下反应:
- 贫血
- 食欲减退
- 出血和瘀伤(血小板减少症)
- 便秘
- 谵妄
- 腹泻
- 水肿(肿胀)
- 疲劳
- 男性生育问题
- 女性生育问题
- 脱发
- 感染和中性白细胞减少
- 淋巴水肿
- 记忆力和注意力变化
- 口腔和咽喉问题
- 恶心和呕吐
- 神经问题(周围神经病变)
- 疼痛
- 男性的性健康问题
- 女性的性健康问题
- 皮肤和指甲变化
- 睡眠变化
- 泌尿系统变化
关于癌症治疗副作用的相关信息可以参考儿童舒缓治疗及安宁护理部分的 3. 症状管理 以上列出的副作用因人而异,即使接受完全相同的治疗,副作用也可能不同。所以孩子如果出现任何副作用,及时跟医护人员沟通。
预后及后续治疗
骨肉瘤15岁以下患者的5年生存率约76%,15-19岁患者的5年生存率约为66%。
1. 影响预后的因素
(1)肿瘤在体内的位置以及肿瘤是否在一个以上的骨骼中形成:发生于四肢一般好于发生于轴向骨骼,四肢肿瘤又以发生在远端的预后较好。
(2)肿瘤的大小:肿瘤较小的预后较好。
(3)肿瘤是否已经扩散到身体的其他部位和扩散的部位:没有转移的患者预后更好。有转移的患者预后取决于转移部位、数量和转移灶是否可以手术切除。
(4)肿瘤的类型(基于肿瘤细胞在显微镜下的形态)。
(5)诊断时患者的年龄和体重:发病时小于18岁的患者预后好于成年后发病的患者。
(6) 患者是否曾接受过其他肿瘤的治疗。
(7)肿瘤是否引起了骨折。没有病理性骨折发生的患者整体预后较好。
(8)患者是否有某些遗传疾病。
(9)肿瘤对化疗的响应:有多少肿瘤细胞被化疗杀死。术前的辅助化疗诱导的肿瘤坏死比例越高则预后越好。
(10)有多大部分肿瘤通过手术取出:肿瘤在手术中可以完全切除的预后较好。
(11) 肿瘤是否在诊断后2年内复发。
2. 观察复发
当治疗结束后,医生会希望继续密切关注患者。按时进行每一次的门诊随访是很重要的。在每次随访之中,医生会询问患者可能遇到的问题,并通过体检、实验室检查或X光和其他影像学检查来寻找肿瘤的迹象或治疗的副作用。几乎所有的治疗手段都有副作用。部分可能持续数周至数月,其他的可能伴随一生。
如果进行了大型骨科手术,坚持进行康复和物理疗法对于患者尽可能重获运动和独立生活能力是很重要的。
3. 管理长期和远期副作用
3.1 骨肉瘤患者的社交、情感和其他问题
很多骨肉瘤发生在青少年时期或者成年早期,这是人一生中非常敏感的时期。骨肉瘤和它的治疗可能对一个人的外表和对自己身体的认识有深远的影响,也会影响他们如何完成日常生活,如学业、工作和娱乐活动。这些影响经常在治疗的第一年是最大的,但是也可能在有些人身上持续很久。
有些儿童和青少年在治疗中和治疗后有情感和心理问题。根据年龄的不同,他们可能在正常生活和学业任务方面存在问题。这些常常可以通过支持和鼓励克服。
肿瘤护理团队建议学龄儿童和青少年尽可能多地去学校,这可以帮助他们维持日常生活并且使他们的朋友了解情况发展。朋友可以是重要的支持来源,但是患儿和父母应该知道有些人对肿瘤有误解和恐惧。
一些医院可能会向新患者介绍完成治疗的患者的项目。这可以给新患者一些对治疗中和治疗后情况的预期。此外看见另一个骨肉瘤患者情况良好也常常会增加治疗信心。鼓励患者参加田径运动和充分利用四肢的活动,很多截肢或者装有假肢的患者最终能够参与田径运动。
父母和其他家庭成员也可能在情感或者其他方面被影响。常见的家庭问题包括经济压力、居住在医院附近、失去工作的可能性、对家庭教育的需要等。
在治疗过程中,患者和家庭倾向于把注意力集中在熬过和战胜肿瘤的方方面面,但是一旦治疗结束,大量的情感问题可能增加,很多还会持续很久,可能包括:
- 面对治疗后身体上的变化
- 担心肿瘤复发或者新的健康问题出现
- 对于自己得了肿瘤、不得不面对治疗感到愤懑
- 担心被差别对待或者歧视(被朋友、同学、同事、雇主等)
- 对约会、婚姻和随后成家产生忧虑
没有人主动选择去患骨肉瘤,但是对于很多儿童和青少年,这一经历可能逐渐变为积极因素,有助于建立强烈的自我价值意识。其他人可能经历一段更艰难的时间去康复,适应其后的生活,从而继续向前。治疗后发生焦虑、抑郁或者其他情绪反应是正常的,但是过度焦虑、抑郁或者愤怒会影响一个年轻人很多方面的成长,可能涉及人际关系、学业、事业和生活的其他方面。
3.2 骨肉瘤治疗远期和长期的影响
很多罹患骨肉瘤的年轻人现在能够生存下来。但是治疗可能会影响他们以后的生活,所以随着他们的成长密切关注健康问题在近些年非常重要。
正如年幼肿瘤患者的治疗是一个非常特殊的过程一样,他们的康复和护理过程也是。问题发现越早,治疗可能越有效。
治疗的长期影响,取决于很多因素,例如肿瘤的类型、接受治疗的类型、治疗的强度和剂量,以及接受治疗时候的年龄。手术的晚期影响可能小至伤疤、大至失去截肢,因而需要物理康复治疗和情感适应。其他远期影响可能包括:
(2)失去听力:特定的化疗药物导致;
(3)生长发育缓慢:骨骼方面或者整体;
(4)年幼儿童的学习问题;
(5)性发育和生育能力的改变:骨肉瘤治疗后出现生育能力问题并不常见,但是还是可能发生的。年长女童或者成年女人在化疗中可能会发生月经周期的变化,但是治疗后正常的周期会恢复。男孩和男人可能暂时失去产生精子的能力,通常这一能力会恢复,但是精子数量可能还是很低。针对盆骨的放疗可能会损伤生育器官从而影响生育能力。可以与你或者你孩子的医生在治疗前讨论不育风险,并且咨询是否有办法保存生育能力,例如精子库;
(6)出现第二种肿瘤:在少数情况下,有些化疗会导致骨肉瘤治愈后多年出现第二种肿瘤(如白血病)。放疗也可能增加在作用位点新肿瘤发病的风险。但是总的来说治疗骨肉瘤的重要性超过这一小小的风险。
关于远期副作用的更多资讯请查看儿童肿瘤治疗远期效应。
就诊提问
与肿瘤治疗团队进行坦率和开放的讨论非常重要。以下问题请注意:
问题1:我(或者我的孩子)的骨肉瘤是什么类型的?这会影响治疗吗?
问题2:是否已经扩散到在其他部位的骨骼?
问题3:骨肉瘤的分期是什么,这意味着什么?
问题4:在我们决定治疗方案以前还需要其他的检查吗?
问题5:针对这种肿瘤您有多少经验?
问题6:我们会需要看其他医生吗?
问题7:我们有哪些治疗选择?
问题8:您推荐什么治疗方案,为什么?
问题9:我们需要多快开始实施治疗?
问题10:治疗需要多久?治疗大概是什么情况,在哪里实施?
问题11:治疗会如何影响我们的日常生活?
问题12:我(我们)需要为治疗做什么准备?
问题13:您建议的治疗方案有什么可能的风险和副作用?
问题14:那些副作用会在治疗后很快出现,那些会晚一些出现?
问题15:治疗会影响我的孩子生长发育吗?
问题16:会不会影响我的(孩子将来的)生育能力吗?
问题17:根据这些治疗方案,肿瘤复发的概率有多大?如果复发我们需要怎么做?
问题18:治疗后的康复方案是什么?
问题19:是否有志愿者团体或者经历过类似情况的其他家庭可以咨询和求助?
参考资料
1. Fuchs B, Valenzuela RG, Petersen IA, et al. Ewing's sarcoma and the development of secondary malignancies. Clin Orthop (415): 82-9, 2003.
2. Goldsby R, Burke C, Nagarajan R, et al. Second solid malignancies among children, adolescents, and young adults diagnosed with malignant bone tumors after 1976: follow-up of a Children's Oncology Group cohort. Cancer 113 (9): 2597-604, 2008.
3. Bhatia S, Krailo MD, Chen Z, et al. Therapy-related myelodysplasia and acute myeloid leukemia after Ewing sarcoma and primitive neuroectodermal tumor of bone: A report from the Children's Oncology Group. Blood 109 (1): 46-51, 2007
4. Kushner BH, Heller G, Cheung NK, et al. High risk of leukemia after short-term dose-intensive chemotherapy in young patients with solid tumors. J Clin Oncol 16 (9): 3016-20, 1998.
5. Ginsberg JP, Goodman P, Leisenring W, et al. Long-term survivors of childhood Ewing sarcoma: report from the childhood cancer survivor study. J Natl Cancer Inst 102 (16): 1272-83, 2010.
6. Kuttesch JF Jr, Wexler LH, Marcus RB, et al. Second malignancies after Ewing's sarcoma: radiation dose-dependency of secondary sarcomas. J Clin Oncol 14 (10): 2818-25, 1996.
7. Grier HE, Krailo MD, Tarbell NJ, et al. Addition of ifosfamide and etoposide to standard chemotherapy for Ewing's sarcoma and primitive neuroectodermal tumor of bone. N Engl J Med 348 (8): 694-701, 2003.
8. Leavey PJ, Mascarenhas L, Marina N, et al. Prognostic factors for patients with Ewing sarcoma (EWS) at first recurrence following multi-modality therapy: A report from the Children's Oncology Group. Pediatr Blood Cancer 51 (3): 334-8, 2008.
9. Stahl M, Ranft A, Paulussen M, et al. Risk of recurrence and survival after relapse in patients with Ewing sarcoma. Pediatr Blood Cancer 57 (4): 549-53, 2011.
10. Barker LM, Pendergrass TW, Sanders JE, et al.: Survival after recurrence of Ewing's sarcoma family of tumors. J Clin Oncol 23 (19): 4354-62, 2005.
11. Grier HE, Krailo MD, Tarbell NJ, et al. Addition of ifosfamide and etoposide to standard chemotherapy for Ewing's sarcoma and primitive neuroectodermal tumor of bone. N Engl J Med 348 (8): 694-701, 2003.
12. Juergens C, Weston C, Lewis I, et al. Safety assessment of intensive induction with vincristine, ifosfamide, doxorubicin, and etoposide (VIDE) in the treatment of Ewing tumors in the EURO-E.W.I.N.G. 99 clinical trial. Pediatr Blood Cancer 47 (1): 22-9, 2006.
相关文章
从光头到长发,向日葵小勇士打败尤文肉瘤的故事
生活,就是学会在雨中翩翩起舞。
儿童骨肉瘤和生长痛有什么区别
一般情况下生长痛通过休息即可得到缓解,而骨肉瘤疼痛会随着疾病发展,从早期刺痛逐渐变为较剧烈疼痛
儿童骨肿瘤的原因
儿童骨肿瘤病因多样,主要包括内因和外因
华莹奇主任:儿童骨肿瘤,到底该截肢还是保肢?
2020年7月24日,华莹奇主任举办了“儿童骨肿瘤专家面对面”专题科普直播。
儿童骨肿瘤是癌症吗
儿童良性骨肿瘤,并非癌症;恶性儿童骨肿瘤即癌症








