哪些措施可以预防蒽环类药物的心脏毒性?
文章来源:向日葵儿童 作者:徐佳琳 责任编辑:admin & wuxiu 时间:2019-05-28
上一期,我们提到了临床药物不良反应因人而异,导致这些个体间差异的因素主要有三类:环境、临床和遗传因素(点击此处查看上一期内容:吃了抗癌药以后出现不良反应和副作用,应当如何排查影响因素?)。
在癌症治疗领域,救命良药惨遭毒性限制的例子屡见不鲜,而基因研究可帮助预测结果。
这一期,我们将着重介绍儿科常用广谱化疗药——蒽环类药物的药物基因组学研究。
蒽环类药物(anthracyclines)是一类临床常用的化疗药,包括多柔比星(doxorubicin)、表柔比星(epirubicin)、柔红霉素(daunorubicin)、伊达比星(idarubicin)等,主要用于治疗多种急性白血病,也用于治疗淋巴瘤、软组织和骨肉瘤等各类儿童恶性肿瘤和成人实体瘤。
然而,用药后的心脏毒性限制了这类药物的临床应用——毒性发生率高达57%,而在16%的患儿中,严重心脏毒性会引起心力衰竭——不少患儿甚至不得不因此接受心脏移植。
01
有哪些因素会影响蒽环类
药物的心脏毒性?
蒽环类药物诱发的心脏毒性也与用药剂量,尤其是这类药物在心脏的剂量有关。
已知影响儿童心脏毒性的临床因素,包括:
①病人接受化疗前的心脏功能;
②年龄(<4岁);
③性别(女>男);
④病人曾经接受心脏附近(例如肺部)的放疗;
⑤病人有没有同时使用其他具有心脏毒性的抗癌疗法,比如环磷酰胺、多西他赛和曲妥珠单抗(赫赛汀);
⑥所谓量变产生质变,患儿长期使用蒽环类药物导致累积剂量过大,也会诱发心脏毒性。

02
有哪些措施可以预防蒽环类
药物的心脏毒性?
蒽环类药物在临床上已经应用了半个世纪。因此,在临床实践中,也有一些方法用来预防或减轻它们的心脏毒性。
然而,这些方法并非完美。
例如,临床上有一种制剂(脂质体),可以给药物穿上“隐身衣”,使它们专门攻击肿瘤细胞的同时,不会进入心脏,那么药物在心脏内的蓄积剂量就减少了。但可以想象,这些高科技“隐身衣”的价格高昂,普及面不广。
又如,在用蒽环类药物的同时使用右丙亚胺——一种心脏保护药物来预防心脏毒性。可是右丙亚胺不光会加剧化疗药的骨髓抑制,造成病人严重贫血,它本身还具有致癌性——谁都不希望自己的孩子治好了一种癌症,却不得不开始对付另一种癌症。
更重要的是,在医生们根据已知的环境和临床因素采取预防措施的背景下,蒽环类药物的心脏毒性仍然呈现出很强的个体间差异。
所以遗传因素应该也在不良反应中起到了重要作用。
03
有哪些基因会对蒽环类药物
的心脏毒性产生影响?
加拿大的一群临床药理学家们通过与儿科医生和科学家的合作,对比了两群孩子的基因组成:一群是用药后发生了严重心脏毒性的孩子,另一群则是同期接受同一疗法的治疗、年龄相仿、却在用药后安然无恙的孩子们。
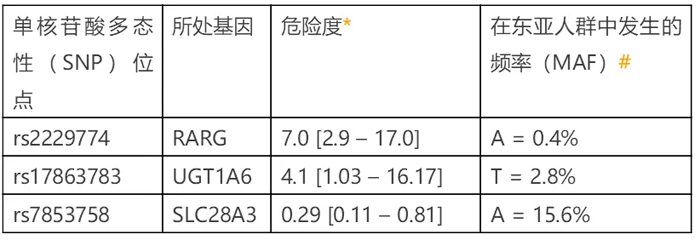
在经过一系列筛选、核查与验证后,他们发现位于三个基因(RARG、UGT1A6和SLC28A3)上的突变会影响蒽环类药物的心脏毒性(见下文表一)。
这些突变属于一类叫做单核苷酸多态性(single nucleotide polymorphism,简写为SNP)的常见遗传变异:顾名思义,就是基因序列上某一个位点的核苷酸发生改变。
SNP广泛存在于人群中,每个人体内都有四五百万个SNP,在遗传学上可以通过不同SNP的排列组合来定义一个人——宏观上,SNP会影响眼睛、头发颜色、鼻梁高度,等等;微观上,正是这些SNP使我们在疾病发生率、用药后的疗效和不良反应等方面出现千差万别。
在上述三个SNP中,前两个(分别位于RARG和UGT1A6基因上)都是危险性的,意味着携带它们的人比普通人在使用蒽环类药物后更容易出现心脏毒性;而最后一个位于SLC28A3基因上的SNP则是保护性的,即携带这个SNP的患者用药后出现心脏毒性的概率低。
注:
*危险度的测量标准是比值比(odds ratio, OR),这是一个统计学概念,以1为衡量标准:OR>1时,OR数值越大,说明携带有这一变异的人发生不良反应的概率越大;OR<1时,数值越小,则说明这一遗传变异可以保护携带者。危险度后面方括号内的数值代表了比值比的可信范围(统计学上叫做95%置信区间)。
#准确地说,此处应为最小等位基因频率(minor allele frequency, MAF)。以T = 2.8%为例,意味着携带有这一危险的遗传变异的人在东亚人群中占比为2.8%*2.8% + 2 * 2.8% * (100% – 2.8%) = 5.52%。换言之,每100个患儿中就有5到6个人携带这一SNP,他们在使用蒽环类药物后就可能产生药物在心脏的蓄积,出现心脏毒性。根据严格的定义,在某一人群中MAF超过1%的遗传变异才能被称为SNP(单核苷酸多态性);在这个研究中,rs2229774是在白人中发现的,它在白人中相对比较常见(MAF = 6.4%),所以属于SNP。
这三个基因中,每一个都与蒽环类药物在体内的传输和转化密切相关。尤其是RARG,会直接影响药物在心脏中的浓度——这也就不难理解RARG基因上的SNP rs2229774为什么危险度这么高了——携带它的患者发生药物不良反应的可能性是其他人的七倍。
04
未来,我们将如何预防蒽环类
药物的心脏毒性?
上述基因研究是在那些已经接受了治疗的孩子们当中完成的。
下一步,加拿大医务工作者们打算更改临床治疗方案:在没有其他有效药物的情况下,对于携带有危险性遗传变异的儿童,临床医生会对他们尽可能减小剂量,使用“隐形衣”脂质体制剂,并使用右丙亚胺保护他们的心脏功能;用药后,医生将每隔一年对患儿的心脏功能进行随访。
而对于携带保护性遗传变异的儿童,医生则不建议运用右丙亚胺,并每隔五年检查一次患儿的心脏功能。
这一工作已经在加拿大展开。截至2018年7月,他们已经使用这一方法治疗了260名儿童癌症患者。科学家和临床药理学家们将长期监测这些患儿的不良反应,而我们也将持续关注他们的监测结果。
期待这项从临床现象出发,经由实验室研究揭露遗传因素对用药潜在影响的研究,最终能回归临床,造福千千万万的癌症患儿。
✿
结语
蒽环类药物因其心脏毒性成为“汝之蜜糖,彼之砒霜”,限制了其临床应用。
对于科学家和医务工作者而言,提前预测不良反应、最大化地发挥药物效用——把正确的药用到正确的病人身上——是一项与开发新型抗癌药物同样重要的任务。
而对于患者和家属,如能提前享受到“基因时代”的红利,通过基因检测预知适合自己的药,那就能最大程度地利用药物而不被其毒性限制——在保障身体健康和生命长度的同时,得到最佳的生命质量。
作者 | 徐佳琳(向日葵志愿者)
排版 | mao
校对 | 何飞 陈臻宇
相关文章
Nature | 单细胞测序技术解开肿瘤分型之迷
美国医生发现三型和四型髓母细胞瘤的主要内部差异,并通过计算推测出三型和四型肿瘤的可能起源和致癌通路。
赵磊副院长:与孩子们一起迎接生命中的挑战,共度难关!
今天为大家奉上山东省肿瘤医院副院长赵磊的致辞视频。
陈若平教授:如何判断手术是否完整切除肿瘤?
儿童胶质瘤百问百答专栏邀请儿童脑肿瘤领域专家,针对性解答儿童胶质瘤方方面面的问题,今天带来第9期~
浙大儿院血液肿瘤内科:变长发化茧成蝶,结疗后重获新生
由『向日葵儿童』公益项目选送的十二家儿童肿瘤相关科室,被正式授予“小儿肿瘤科普教育基地”。
你看见自己身上悄然发生的改变了吗?
到今天为止,我们的28天心理心灵康复之旅已经进行到第7天,第一阶段:身心一体的秘密到这里就结束了。








