质子治疗的优势:针对儿童实体瘤,效果好,副作用还小!
文章来源:向日葵儿童 作者:瑞士专家 责任编辑:admin & gaozx 时间:2019-06-06
写在前面
质子治疗作为一种效果优越的新型放疗方法,颇受家长们的关注。因此,向日葵儿童联系了瑞士保罗·谢尔研究所(Paul Scherrer Institute)质子治疗中心的几位专家,请他们讲讲质子治疗到底该怎么用。下面这篇文章的原文于2018年4月发表于瑞士专业期刊《Info@ Onkologie》,我们经GLS Health的帮助,联系了瑞士保罗·谢尔质子中心和文章作者,经授权为大家整理翻译成了中文。
放疗是儿科肿瘤治疗的重要支柱。质子治疗作为肿瘤放疗中的特殊治疗方式,可以为儿童提供格外温和的治疗手段, 使长期治疗引起的副作用及其它风险最小化。在这篇文章中,我们就来谈谈质子治疗在儿童中应用的可能性及其优势。
划重点
质子治疗能够最大限度地保护对辐射敏感的组织和器官。
质子治疗能够降低二次恶性肿瘤和长期毒性反应的风险。
由于儿童对辐射尤为敏感,因此质子治疗对儿童患者意义重大。
在瑞士,每年大约有200名儿童和青少年被诊断为癌症。其中最为常见的要数白血病(占34%)、中枢神经系统肿瘤(占21%)和淋巴瘤(占11%)。在确诊后,这些肿瘤的治疗通常由不同疗法的组合构成,根据其为实体瘤还是血液瘤,以及肿瘤的分期,而有所不同。
在过去的几十年里,多种方法结合的强化治疗理念使得儿童的治愈率不断提高,如今超过80%的儿童可以治愈。在这些治疗理念中,放疗往往极为重要。约有一半的肿瘤患儿会接受放疗。
然而,这些治疗肿瘤的手段通常对人体毒性很大,并可能导致相当大的长期副作用。为了减少副作用的发生,科学家和医生们正在寻找新的治疗方法和策略。而质子治疗正是这样一种新的放疗方法,它可以显著地减少副作用。
在使用光子(X射线)的传统放疗中,通过技术上的创新,放疗精准性和对相关脏器的保护已经得到了相当大的改善。但由于质子的物理性能更佳,因此和光子相比,质子极有可能会提供更为温和的辐射。不过,必须强调的是,在对肿瘤细胞的损伤方面,质子和光子的生物学作用机制是一样的。
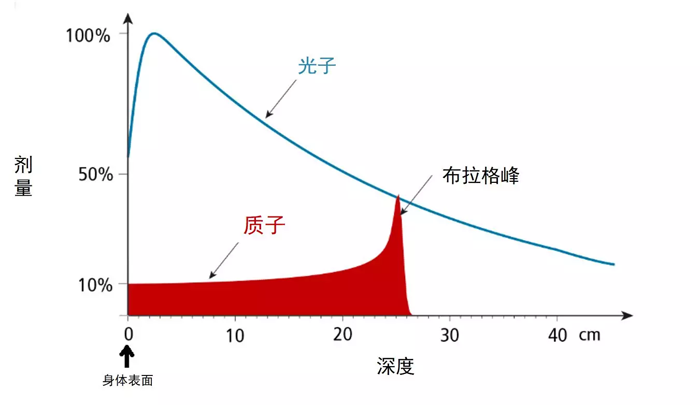
质子是一种基本粒子,是原子核的一部分。它和传统放疗所使用的X射线极为不同,二者进入物质时表示出的物理行为也大相径庭。X射线是一种电磁波,它在进入人体后立即放射出最高剂量的辐射,然后其辐射剂量以指数方式降低,直到离开人体。
而质子则不然。它具有一定的穿透深度,这一深度是由其初始速度决定的。而且,质子在穿透到最深处时才会放射出最大辐射剂量,这个剂量的最大值称为布拉格峰。在布拉格峰之后,辐射剂量急剧下降(见图1)。 借助计算机辅助的辐射规划系统,可以计算出质子进入人体时所需的速度,使布拉格峰的最大值正好位于肿瘤中。 因此,在到达肿瘤之前,质子的辐射剂量很低;而穿过肿瘤之后,健康组织不会受到辐射。 在质子对肿瘤区域以外的辐射剂量显著低于光子, 因而可以最大限度地保护健康组织和肿瘤周围的器官,减少副作用。
儿童的身体对辐射极为敏感。肿瘤治疗中的一大问题就是由化疗和电离辐射(比如X射线)诱发的二次恶性肿瘤。化疗往往会在治疗后的5年内诱发血液疾病,而放疗则可能诱发实体瘤,其发病时间通常在放疗结束后10年以上。
而质子治疗可以减少健康组织中的辐射剂量,因此可以降低二次恶性肿瘤的风险。用质子治疗进行的颅脊轴放疗,其诱发二次肿瘤的风险是光子治疗的8到15分之一。
对颅内肿瘤进行放疗时,对脑组织和周围的器官进行保护尤为重要。目前的研究已经证实,颅内放疗造成的损伤,其严重程度是和辐射剂量及靶区体积相关的。如果将质子和光子辐射进行比较,质子在健康的脑组织中的辐射剂量更小,造成的负担也更少,因此可以更好地保持神经认知功能。
此外,研究表明,颅内放疗损伤的严重程度也和儿童的年龄极为相关。 比如,幼年患者的大脑对辐射就尤为敏感。 对5岁以下的儿童进行颅内放疗,会导致儿童智商显著下降; 而在12岁以上的儿童中,颅内放疗对智商就不再有显著影响。因此,对于低龄儿童来说,质子治疗更是意义重大。
而且,放疗也可能对患者的听力造成永久损伤。 因此,接受放疗的患者可能会有不同程度的听觉恶化,最严重的可能导致听力完全损失。在一项关于接受放疗的患儿的研究中,高达36%的儿童脑瘤长期生存者被诊断出听力障碍。相较于光子治疗,质子治疗可能会对这个问题有所改善。
质子治疗可以更好地保护脑垂体和下丘脑,从而降低因辐射而诱导内分泌缺陷的风险。与光子治疗相比,质子治疗可以使生长激素缺乏的相对风险降低75%,甲状腺功能减退的相对风险降低85%。
适用质子治疗的肿瘤以颅内肿瘤为主。其中最常见的是胚胎瘤,如成神经管细胞瘤、原始神经外胚层肿瘤(PNETs)、星形细胞瘤和室管膜瘤,以及位于脑中蝶鞍区域的肿瘤,如颅咽管瘤和垂体腺瘤。 还有一些较少发生的脑瘤,包括非典型畸胎样/横纹肌样瘤(AT/RT)、脉络丛癌及松果体母细胞瘤。在这些肿瘤中,放疗通常被用作手术切除后的辅助治疗,以优化局部的肿瘤控制。质子治疗可以最大限度地保护肿瘤临近区域的重要器官。对于不能手术的肿瘤,如脑干胶质瘤,治疗则完全依赖于放疗。
瑞士保罗·谢尔研究所对患有室管膜瘤、胶质瘤和非典型畸胎样/横纹肌样瘤的患儿进行了回顾性分析,发现质子治疗有着优良的效果,可以很好地控制肿瘤,并降低副作用率。
如果肿瘤细胞有很高的风险散播到脑脊液中,或已经转移到了中枢神经系统中, 那么除了对原发肿瘤区域进行局部放疗外,还需要对整个脑脊液系统进行颅脊轴放疗。相对于常规放疗,质子治疗在这类治疗中有着明显的优势,在对脊髓脑脊液系统进行放疗时尤为突出。在仅对背部进行放疗时,质子会完全停留在脊柱内。脊柱前部的颈部、胸部、腹部、骨盆组织和器官,则完全不会受到辐射(见图2)。这可以防止各种器官如甲状腺、心脏、肺部和肠道的晚期损伤。
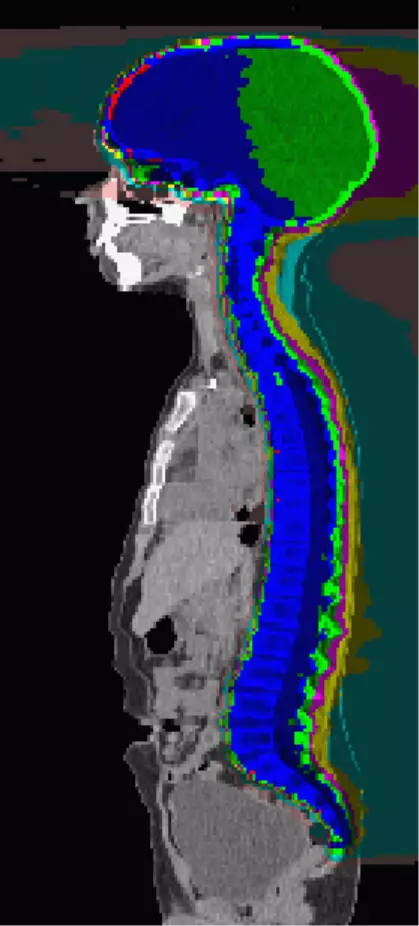
放疗也可以用于治疗颅外肿瘤,通常用于肉瘤(横纹肌肉瘤和尤因肉瘤)和神经母细胞瘤。初期放疗往往是这些实体瘤治疗方案中的一部分。在理想情况下,放疗会使肿瘤缩小,从而更容易切除。随后,放疗通常用于对原发肿瘤部位或残留肿瘤组织进行照射。质子治疗也可用于治疗这些肿瘤,使得健康组织得到更好的保护, 使重要器官受到辐射剂量最小化。 保罗·谢尔研究所也对肉瘤患儿的治疗进行了回顾性评估, 发现质子治疗表示出了良好的治疗耐受性和令人欣喜的肿瘤控制率。
在癌症患儿的治疗中,放疗带来的风险一直是大家关心的问题。相较于传统的放疗方式,质子治疗能够在损伤肿瘤细胞的同时,最大限度地保护对辐射敏感的组织和器官,降低二次恶性肿瘤和长期毒性反应的风险。 由于儿童对辐射尤为敏感性,因此质子治疗对儿童患者更是意义重大。目前,在瑞士保罗·谢尔研究所,质子治疗主要用于颅内实体瘤和部分颅外实体瘤的治疗,并取得了很好的效果。希望未来,随着科学研究和技术的发展,更多的孩子可以从中受益,得到更美好的未来!
✿
作者简介
Marc Walser医生是瑞士保罗·谢尔研究所质子治疗中心的首席放射肿瘤学家。Marc Walser医生毕业于苏黎世大学,并在埃尔朗根大学医院接受了住院医师培训。他是欧洲治疗放射学和肿瘤学会(ESTRO)的成员,也是多份出版物的合著作者。
Barbara Bachtiary医生是一位经验丰富的放射肿瘤学家。她是奥地利放射肿瘤学、放射生物学和医学放射物理学(ÖGRO)和欧洲治疗放射学和肿瘤学会(ESTRO)的成员,曾荣获多项奖学金和各种奖项,且著有众多出版作品。
Damien C. Weber教授是瑞士保罗·谢尔研究所质子治疗中心的主席,是神经肿瘤学和儿科领域的专家。Weber教授在日内瓦大学取得了医学博士学位和教学资格,此后在哈佛大学东北质子治疗中心参与研究与临床医疗,并在此接受了放射肿瘤学方面的培训。自2013年起,Weber教授一直担任瑞士保罗·谢尔研究所质子治疗中心的主席。目前,他还同时担任伯尔尼和苏黎世大学(University of Bern and Zurich)的教授、欧洲治疗放射学和肿瘤学会放射肿瘤学分会的主席,以及欧洲治疗放射学和肿瘤学会粒子治疗网络的创始人之一。他还是欧洲治疗放射学和肿瘤学会科学委员会的成员之一,也是许多其他国际学会(如瑞士放射肿瘤学科学学会和国际小儿肿瘤学学会)的活跃成员。
研究所简介
瑞士保罗·谢尔研究所是欧洲第一个将质子治疗应用于临床的中心,也是瑞士唯一可以提供质子治疗的机构。保罗·谢尔研究所发明了质子治疗中的点扫描技术,可以根据肿瘤的具体形状,逐点对肿瘤进行扫描照射,在肿瘤形状往往不规则的前提下,保证对肿瘤每个部分都进行有效的辐射,同时对周围组织提供最大的保护。该技术现已应用到所有现代质子治疗系统中。
参考文献:
1. Gatta G. et al.: Childhood cancer survival in Europe 1999–2007: results of EUROCARE-5—a population-based study. Lancet Oncol 2014; 15(2): 35-47
2. Morris EB et al.: Survival and late mortality in long-term survivors of pediatric CNS tumors. J Clin Oncol 2007; 25(12): 1532–1538.
3. Miralbell R et al.: Potential reduction of the incidence of radiation-induced second cancers by using proton beams in the treatment of pediatric tumors. Int J Radiat Oncol Biol Phys 2002; 54(3): 824–829.
4. Pulsifer MB et al.: Early Cognitive Outcomes Following Proton Radiation in Pediatric Patients with Brain and Central Nervous System Tumors. Int J Radiat Oncol Biol Phys 2015; 93(2): 400–407.
5. Greenberger BA et al.: Clinical outcomes and late endocrine, neurocognitive, and visual profiles of proton radiation for pediatric low-grade gliomas. Int J Radiat Oncol Biol Phys 2014; 89(5): 1060–1068.
6. Merchant TE et al.: Late effects of conformal radiation therapy for pediatric patients with low-grade glioma: prospective evaluation of cognitive, endocrine, and hearing deficits. J Clin Oncol 2009; 27(22): 3691–3697.
7. Brinkman TM et al.: Treatment-induced hearing loss and adult social outcomes in survivors of childhood CNS and non-CNS solid tumors: Results from the St. Jude Lifetime Cohort Study. Cancer 2015; 121(22): 4053–4061.
8. Vatner RE et al.: Endocrine Deficiency as a Function of Proton Radiation Dose to the Hypothalamus in Children with Brain Tumors. Int J Radiat Oncol Biol Phys 2016; 96(2): 231–232.
9. Ares C et al.: Pencil beam scanning proton therapy for pediatric intracranial ependymoma. J Neurooncol 2016; 128(1): 137–145.
10. Badiyan SN et al.: Clinical and Radiologic Outcomes in Adults and Children Treated with Pencil-Beam Scanning Proton Therapy for Low-Grade Glioma. Int J Particle Ther 2017; 3(4): 450–460.
11. Weber DC et al.: Tumor control and QoL outcomes of very young children with atypical teratoid/rhabdoid tumor treated with focal only chemo-radiation therapy using pencil beam scanning proton therapy. J Neurooncol 2015; 121(2): 389–397.
12. Leiser D et al.: Tumour control and Quality of Life in children with rhabdomyosarcoma treated with pencil beam scanning proton therapy. Radiother Oncol 2016; 120(1): 163-168
13. Weber DC et al.: Pencil Beam Scanning Proton Therapy for Pediatric Parameningeal Rhabdomyosarcomas: Clinical Outcome of Patients Treated at the Paul Scherrer Institute. Pediatr Blood Cancer 2016; 63(10): 1731–1736.
14. Weber DC et al.: Pencil beam scanned protons for the treatment of patients with Ewing sarcoma. Pediatr Blood Cancer 2017; 64(12): (Doi: 10.1002/pbc.26688)
作者 | Marc Walser
Barbara Bachtiary
Damien C. Weber
翻译 | 严青,生物学博士
联络 | 吕宁,瑞士医疗咨询/罕见病公益组织
校对 | 秀秀 忽亚丽
相关文章
中国18%的肿瘤患儿未被诊断?到底多少孩子生病?
儿童肿瘤诊断率在全球,尤其是在不发达国家被大大低估。根据测算,东亚地区儿童肿瘤的未诊率大约在18%。
儿童癌症是绝症吗?不,治疗效果要比成人好很多
遗憾的是,这一理念被知晓的程度极低。事实上,一些儿童肿瘤是完全能够治好的,治愈率也比成人高得多。
儿童重疾险如何选择?
这一篇我们将介绍家长最为关心的重疾险,以及常见的保险配置误区。
手术中,肉眼全切、次全切、部分切除,分别指什么?
手术中,肉眼全切、次全切、部分切除,分别指什么?
“疟疾治愈癌症”持续发酵
在营销号的推波助澜下,患者已经把临床试验咨询电话打爆了!








